1.Larutan dapat diklasifikasikan misalnya berdasarkan fase zat terlarut dan pelarutnya. Tabel berikut menunjukkan contoh-contoh larutan berdasarkan fase komponen-komponennya.
| Contoh larutan | Zat terlarut | |||
|---|---|---|---|---|
| Gas | Cairan | Padatan | ||
| Pelarut | Gas | Udara (oksigen dan gas-gas lain dalam nitrogen) | Uap air di udara (kelembapan) | Bau suatu zat padat yang timbul dari larutnya molekul padatan tersebut di udara |
| Cairan | Air terkarbonasi (karbon dioksida dalam air) | Etanol dalam air; campuran berbagai hidrokarbon (minyak bumi) | Sukrosa (gula) dalam air; natrium klorida (garam dapur) dalam air; amalgam emas dalam raksa | |
| Padatan | Hidrogen larut dalam logam, misalnya platina | Air dalam arang aktif; uap air dalam kayu | Aloi logam seperti baja dan duralumin | |
1.1 Larutan Elektrolit
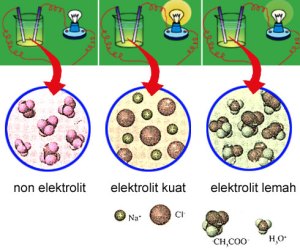
Larutan elektrolit merupakan larutan yang dibentuk dari zat elektrolit. Sedangkan zat elektrolit itu sendiri merupakan zat-zat yang di dalam air terurai membentuk ion-ionnya. Zat elektrolit yang terurai sempurna di dalam air disebut Elektrolit Kuat dan larutan yang dibentuknya disebut Larutan Elektrolit Kuat. Zat elektrolit yang hanya terurai sebagian membentuk ion-ionnya di dalam air disebut Elektrolit Lemah dan larutan yang dibentuknya disebut Larutan Elektrolit Lemah.
1.2 Larutan Non-Elektrolit
Larutan non elektrolit merupakan larutan yang dibentuk dari zat non elektrolit. Sedangkan zat non elektrolit itu sendiri merupakan zat-zat yang di dalam air tidak terurai dalam bentuk ion-ionnya, tetapi terurai dalam bentuk molekuler.
1.3 Membedakan Larutan Elektrolit dan Larutan Non Elektrolit
Larutan elektolit dan non elektrolit dapat dibedakan dengan jelas dari sifatnya yaitu penghantaran Listrik.
a). Larutan elektrolit dapat menghantarkan listrik.
Hal ini untuk pertama kalinya diterangkan oleh Svante August Arrhenius(1859-1927), seorang ilmuwan dari Swedia. Arrhenius menemukan bahwa zat elektrolit dalam air akan terurai menjadi partikel-partikel berupa atom atau gugus atom yang bermuatan listrik. Karena secara total larutan tidak bermuatan, maka jumlah muatan positif dalam larutan harus sama dengan muatan negatif.
Atom atau gugus atom yang bermuatan listrik itu dinamai ion. Ion yang bemuatan positif disebut kation, sedangkan ion yang bermuatan negatif disebut anion. Pembuktian sifat larutan elektrolit yang dapat menghantarkan listrik ini dapat diperlihatkan melalui eksperimen. Zat-zat yang tergolong elektrolit yaitu asam, basa, dan garam.
Contoh larutan elektrolit kuat : HCl, HBr, HI, HNO3, dan lain-lain
Contoh larutan elektrolit lemah :CH3COOH, Al(OH)3 dan Na2CO3
b). Larutan non elektrolit tidak dapat menghantarkan listrik.
Adapun larutan non elektrolit terdiri atas zat-zat non elektrolit yang tidak dilarutkan ke dalam air tidak terurai menjadi ion ( tidak terionisasi ). Dalam larutan, mereka tetap berupa molekul yang tidak bermuatan listrik. Itulah sebabnya larutan non elektrolit tidak dapat menghantarkan listrik. Pembuktian sifat larutan non elektrolit yang tidak dapat menghantarkan listrik ini dapat diperlihatkan melalui eksperimen.
Contoh larutan non elektrolit : Larutan Gula (C12H22O11), Etanol (C2H5OH), Urea (CO(NH)2), Glukosa (C6H12O6), dan lain-lain
1.4 Kekuatan Elektrolit
Kekuatan suatu elektrolit ditandai dengan suatu besaran yang disebut derajat ionisasi (α)
Keterangan :
Elektrolit kuat memiliki harga α = 1, sebab semua zat yang dilarutkan terurai menjadi ion.
Elektrolit lemah memiliki harga α<1, sebab hanya sebagian yang terurai menjadi ion.
Adapun non elektrolit memiliki harga α = 0, sebab tidak ada yang terurai menjadi ion.
Elektrolit kuat : α = 1(terionisasi sempurna)
Elektrolit lemah : 0 < α < 1 (terionisasi sebagian)
Non Elektrolit : α = 0 (tidak terionisasi)
1.5 Reaksi Ionisasi Elektrolit Kuat
Larutan yang dapat memberikan lampu terang, gelembung gasnya banyak, maka laurtan ini merupakan elektrolit kuat. Umumnya elektrolit kuat adalah larutan garam. Dalam proses ionisasinya, elektrolit kuat menghasilkan banyak ion maka = 1 (terurai senyawa), pada persamaan reaksi ionisasi elektrolit kuat ditandai dengan anak panah satu arah ke kanan.
Perlu diketahui pula elektrolit kuat ada beberapa dari asam dan basa.
Contoh :
NaCl (aq)
KI (aq)
Ca(NO3)2(g) Na+(aq) + Cl-(aq)
K+(aq) + I-(aq)
Ca2+(aq) + NO3-(aq)
Di bawah ini diberikan kation dan anion yang dapat membentuk elektrolit kuat.
Kation : Na+, L+, K+, Mg2+, Ca2+, Sr2+, Ba2+, NH4+
Anion : Cl-, Br-, I-, SO42-, NO3-, ClO4-, HSO4-, CO32-, HCO32-
1.6 Reaksi Ionisasi Elektrolit Lemah
Larutan yang dapat memberikan nyala redup ataupun tidak menyala, tetapi masih terdapat gelembung gas pada elektrodanya maka larutan ini merupakan elekrtolit lemah. Daya hantarnya buruh dan memiliki á (derajat ionisasi) kecil, karena sedikit larutan yang terurai (terionisasi). Makin sedikit yang terionisasi, makin lemah elektrolit tersebut. Dalam persamaan reaksi ionisasi elektrolit lemah ditandai dengan panah dua arah (bolak-balik) artinya tidak semua molekul terurai (ionisasi tidak sempurna)
Contoh:
CH3COOH(aq)
NH4OH(g) CH3COO-(aq) + H+(aq)
NH4+(aq) + OH-(aq)
2. Cara Larutan Elektrolit Menghantarkan Arus Listrik
Pada tahun 1884, Svante Arrhenius, ahli kimia terkenal dari Swedia mengemukakan teori elektrolit yang sampai saat ini teori tersebut tetap bertahan padahal ia hampir saja tidak diberikan gelar doktornya di Universitas Upsala, Swedia, karena mengungkapkan teori ini. Menurut Arrhenius, larutan elektrolit dalam air terdisosiasi ke dalam partikel-partikel bermuatan listrik positif dan negatif yang disebut ion (ion positif dan ion negatif) Jumlah muatan ion positif akan sama dengan jumlah muatan ion negatif, sehingga muatan ion-ion dalam larutan netral. Ion-ion inilah yang bertugas mengahantarkan arus listrik.
” Larutan elektrolit dapat menghantarkan listrik karena mengandung ion-ion yang dapat bergerak bebas. Ion-ion itulah yang menghantarkan arus listrik melalui larutan”.
Larutan yang dapat menghantarkan arus listrik disebut larutan elektrolit.
Larutan ini memberikan gejala berupa menyalanya lampu atau timbulnya gelembung gas dalam larutan.
Larutan elektrolit mengandung partikel-partikel yang bermuatan (kation dan anion). Berdasarkan percobaan yang dilakukan oleh Michael Faraday, diketahui bahwa jika arus listrik dialirkan ke dalam larutan elektrolit akan terjadi proses elektrolisis yang menghasilkan gas. Gelembung gas ini terbentuk karena ion positif mengalami reaksi reduksi dan ion negatif mengalami oksidasi. Contoh, pada laruutan HCl terjadi reaksi elektrolisis yang menghasilkan gas hidrogen sebagai berikut.
HCl(aq)→ H+(aq) + Cl-(aq)
Reaksi reduksi : 2H+(aq) + 2e- → H2(g)
Reaksi oksidasi : 2Cl-(aq) → Cl2(g) + 2e-
Larutan elektrolit terdiri dari larutan elektrolit kuat contohnya HCl, H2SO4, dan larutan elektrolit lemah contohnya CH3COOH, NH3, H2S.
Larutan elektrolit dapat bersumber dari senyawa ion (senyawa yang mempunyai ikatan ion) atau senyawa kovalen polar (senyawa yang mempunyai ikatan kovalen polar)
Zat elektrolit yang terurai dalam air menjadi ion-ion :
HaCl (s) Na+ (aq) + Cl- (aq)
HCl (g) H+ (aq) + Cl- (aq)
H2SO4 (aq) 2H+ (aq) + SO4 2- (aq)
HaOH (s) Na+ (aq) + OH- (aq)
CH3COOH (l) CH3COO- (aq) + H+ (aq)
Zat non elektrolit yang tidak terurai menjadi ion-ion, tapi tetap berupa molekul
C2H5OH (l) C2H5OH (aq)
CO(NH2)2 (s) CO(NH2)2 (aq)
Reaksi peruraian disebut elektrolisis
Reaksi reduksi : pada katode, electron ditangkap oleh ion
Reaksi oksidasi : pada anode, ion akan melepaskan electron
Berdasarkan pelepasan dan pengikatan oksigen
Reaksi oksidasi : reaksi pengikatan oksigen
Contoh : C6H1206 CO2 + 6H2O
3S + 2KClO3 2KCl + 3SO2
Reaksi Reduksi :Reaksi pelepasan oksigen
Contoh : Fe2O3 + 3CO 2Fe2 + 3CO2
CuO + H2 Cu + H2O
3. Hubungan Keelektrolitan dengan ikatan kimia
3.1 Senyawa Ion
Sebagai contoh dari kegiatan percobaan yang tergolong larutan elektrolit yang berikatan ion adalah garam dapur.
Dapatkah Anda membedakan daya hantar listrik untuk garam pada saat kristal, lelehan dan larutan?
Cobalah perhatikan uraian berikut.
NaCl adalah senyawa ion, jika dalam keadaan kristal sudah sebagai ion-ion, tetapi ion-ion itu terikat satu sama lain dengan rapat dan kuat, sehingga tidak bebas bergerak. Jadi dalam keadaan kristal (padatan) senyawa ion tidak dapat menghantarkan listrik, tetapi jika garam yang berikatan ion tersebut dalam keadaan lelehan atau larutan, maka ion-ionnya akan bergerak bebas, sehingga dapat menghantarkan listrik.
Pada saat senyawa NaCl dilarutkan dalam air, ion-ion yang tersusun rapat dan terikat akan tertarik oleh molekul-molekul air dan air akan menyusup di sela-sela butir-butir ion tersebut (proses hidasi) yang akhirnya akan terlepas satu sama lain dan bergerak bebas dalam larutan.
Yang termasuk ke dalam senyawa ion adalah senyawa basa dan garam.
NaCl (s) + air Na+ (aq) + Cl-(aq)
3.2 Senyawa Kovalen
Senyawa kovalen terbagi menjadi senyawa kovalen non polar misalnya : F2, Cl2, Br2, I2, CH4 dan kovalen polar misalnya : HCl, HBr, HI, NH3.
Dari hasil percobaan, hanya senyawa yang berikatan kovalen polarlah yang dapat menghantarkan arus listrik. Bagaimanakah hal ini dapat dijelaskan?
Kalau kita perhatikan, bahwa HCl merupakan senyawa kovalen di atom bersifat polar, pasangan elektron ikatan tertarik ke atom Cl yang lebih elektro negatif dibanding dengan atom H. Sehingga pada HCl, atom H lebih positif dan atom Cl lebih negatif.
Struktur lewis:
Reaksi ionisasi nya adalah sebagai berikut : HCL(aq) H+(aq) + Cl-(aq)
Jadi walaupun molekul HCl bukan senyawa ion, jika dilarutkan ke dalam air maka larutannya dapat menghantarkan arus listrik karena menghasilkan ion-ion yang bergerak bebas.
HCl(g) + H2O(l)
HCl(g)
HCl(g) H3O+(aq) + Cl-(aq)
H3O+ + Cl-(g)
H+(aq) + Cl-(aq)
Apakah HCl dalam keadaan murni dapat menghantarkan arus listrik? Karena HCl dalam keadaan murni berupa molekul-molekul tidak mengandung ion-ion, maka cairan HCl murni tidak dapat menghantarkan arus listrik.
4. Kesimpulan
Dari penjelasan di atas maka dapat disimpulkan bahwa suatu larutan akan dapat menghantarkan listrik apabila lrutan tersebut memiliki ion-ion yang bergerak bebas, tapi apabila ion-ion berbentuk rapat dan kuat, sehingga tidak dapat bergerak bebas maka larutan tersebut tidak dapat menghantarkan listrik.










maasih bro,, bLognya membantu. GBU